
- Autor Miles Stephen stephen@answers-science.com.
- Public 2023-12-15 23:40.
- Modificat ultima dată 2025-01-22 17:08.
Suma celor număr de protoni și neutroni dintr-un atom se numește numar de masa . Masă atomică nu este niciodată un număr întreg număr din mai multe motive: The masă atomică raportat pe a tabelul periodic este media ponderată a tuturor izotopilor naturali. Fiind o medie, ar fi cel mai puțin probabil să fie un întreg număr.
În mod similar, vă puteți întreba, de ce tabelul periodic este aranjat după număr atomic în loc de masă?
Numar atomic este număr de protoni în nucleul fiecăruia atomii elementului . Acea număr este unic pentru fiecare element . Masă atomică este determinată de număr de protoni și neutroni combinați.
În plus, de ce greutatea atomică a bromului enumerată în tabelul periodic nu este un număr întreg? Explicație: Toate elementele au un înveliș de izotopi și masă atomică citat pe Tabelul periodic este MEDIA PONDERATĂ a izotopilor individuali La o primă aproximare brom este format din DOI izotopi: 51% 79Br și 49% 81Br.
Știți, de asemenea, de ce masa atomică a unui element listat în tabelul periodic este o masă medie ponderată?
The masă atomică este o medie ponderată dintre toți izotopii acestuia element , în care masa al fiecărui izotop este înmulțit cu abundența acelui izotop particular. ( Masă atomică mai este denumită greutate atomica , dar termenul " masa " este mai precis.)
Cum se determină masele din tabelul periodic?, dar au diferite masa numere (numărul total de protoni și neutroni) dându-le atomice diferite mase.
Recomandat:
Ce înseamnă numerele din tabelul periodic?

Numărul de deasupra simbolului este masa atomică (sau greutatea atomică). Acesta este numărul total de protoni și neutroni dintr-un atom. Numărul de sub simbol este numărul atomic și acesta reflectă numărul de protoni din nucleul atomului fiecărui element. Există 18 coloane principale de elemente în tabelul periodic
Cum se determină masa atomică medie afișată în tabelul periodic?

Masa atomică medie pentru un element este calculată prin însumarea maselor izotopilor elementului, fiecare înmulțit cu abundența sa naturală pe Pământ. Când efectuați calcule de masă care implică elemente sau compuși, utilizați întotdeauna masa atomică medie, care poate fi găsită în tabelul periodic
Ce sunt numerele naturale numerele întregi și numerele raționale?
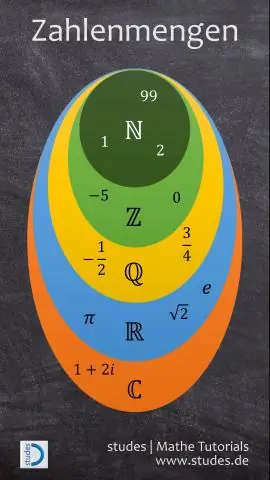
Numerele reale sunt clasificate în principal în numere raționale și iraționale. Numerele raționale includ toate numerele întregi și fracțiile. Toate numerele întregi negative și numerele întregi alcătuiesc mulțimea numerelor întregi. Numerele întregi cuprind toate numerele naturale și zero
Care număr nu este comun între numerele naturale și numerele întregi?

Zero nu are o valoare pozitivă sau negativă. Cu toate acestea, zero este considerat un număr întreg, ceea ce, la rândul său, îl face un număr întreg, dar nu neapărat un număr natural
Cum rezolvi numerele complexe și numerele imaginare?

Numerele complexe au forma a+bi a + b i, unde a și b sunt numere reale și i este rădăcina pătrată a lui −1. Toate numerele reale pot fi scrise ca numere complexe prin setarea b=0. Numerele imaginare au forma bi și pot fi scrise și ca numere complexe prin stabilirea a=0
