
- Autor Miles Stephen stephen@answers-science.com.
- Public 2023-12-15 23:40.
- Modificat ultima dată 2025-01-22 17:08.
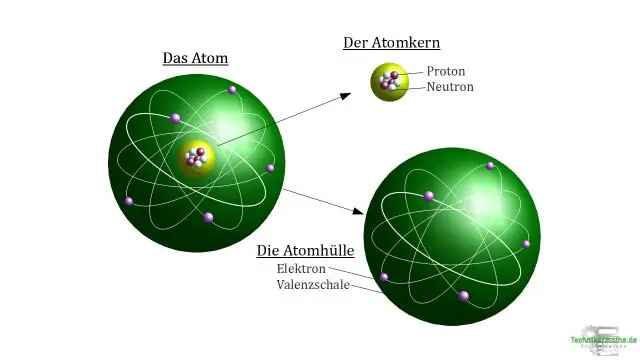
Un învelișul de electroni este partea exterioară a unui atom in jurul atomic nucleu. Este locul unde electron s sunt și este un grup de atomic orbitali cu aceeași valoare a numărului cuantic principal n.
În consecință, câte învelișuri de electroni există?
Fiecare coajă poate conține doar un număr fix de electroni : The primul coajă poate ține până la două electroni , cel al doilea coajă poate ține până la opt (2 + 6) electroni , cel al treilea coajă poate ține până la 18 (2 + 6 + 10) și așa mai departe. The formula generală este aceea cel al n-lea coajă poate sa în principiu ține până la 2 (n2) electroni.
În al doilea rând, ce este shell-ul KLMN? K desemnează primul coajă (sau nivelul de energie), L al doilea coajă , M, al treilea coajă , si asa mai departe. Cu alte cuvinte, KLMN Notația (OP) indică doar numărul de electroni pe care un atom îi are cu fiecare număr cuantic principal (n). Notația SPDF subîmparte fiecare coajă în subînvelișurile sale.
Ținând cont de acest lucru, ce sunt învelișurile de electroni și orbitalii?
Fiecare învelișul de electroni constă dintr-unul sau mai multe subshell-uri și fiecare subshell este format din unul sau mai multe orbitali . Se afirmă adesea că electroni în același învelișul de electroni au aceleași niveluri de energie. De exemplu, s orbitali în primele trei învelișuri de electroni vor fi denumite 1, 2 și 3 orbitali.
De ce sunt doar 2 electroni în primul înveliș?
Acest prima coajă are numai un subshell (etichetat 1s) și poate conține maximum 2 electroni . Acesta este motivul pentru care există două elemente în primul rândul tabelului periodic (H & He). Pentru că prima coajă poate sa numai ține maximum de 2 electroni , al treilea electron trebuie să intre în al doilea coajă.
Recomandat:
Care este sarcina unui atom care câștigă electroni?
Un ion este un atom care a câștigat sau a pierdut unul sau mai mulți electroni și, prin urmare, are o sarcină negativă sau pozitivă. Un cation este un atom care a pierdut un electron de valență și, prin urmare, are mai mulți protoni pozitivi decât electroni negativi, deci este încărcat pozitiv
Care sunt particulele fundamentale ale unui atom?

Atomii sunt formați din protoni, neutroni și electroni. Aceste particule subatomice clasice constau din particule fundamentale sau elementare de materie. Deoarece sunt și particule de materie, au dimensiune și masă. Particulele fundamentale sunt grupate ca leptoni și quarci
Care sunt cele două părți principale ale unui atom?

Cele două componente principale ale unui atom sunt nucleul și norul de electroni. Nucleul conține particule subatomice neutre și încărcate pozitiv, în timp ce norul de electroni conține particule minuscule încărcate negativ
Cum sunt spectrele de emisie dovezi pentru învelișurile de electroni în modelul Bohr?

Prezența doar a anumitor linii în spectrele atomice a însemnat că un electron poate adopta doar anumite niveluri de energie discrete (energia este cuantificată); de unde ideea de învelișuri cuantice. Frecvențele fotonilor absorbite sau emise de un atom sunt fixate de diferențele dintre nivelurile de energie ale orbitelor
Cum sunt dovezile spectrului de emisie pentru învelișurile de electroni?

Prezența doar a anumitor linii în spectrele atomice a însemnat că un electron poate adopta doar anumite niveluri de energie discrete (energia este cuantificată); de unde ideea de învelișuri cuantice. Frecvențele fotonilor absorbite sau emise de un atom sunt fixate de diferențele dintre nivelurile de energie ale orbitelor
