
- Autor Miles Stephen stephen@answers-science.com.
- Public 2023-12-15 23:40.
- Modificat ultima dată 2025-01-22 17:08.
Da Na+ este mai mic decât N / A deoarece Na+ este format atunci când un electron este pierdut din N / A atom, Astfel sarcina nucleară efectivă crește bcz numărul de protoni depășește numărul de electroni. Acest lucru are ca rezultat aducerea învelișului de valență puțin mai aproape de nucleu din cauza unei tracțiuni nucleare foarte puternice.
Pe lângă aceasta, care are o rază mai mare Na+ sau NE?
Ne vom avea raza mai mare decât Na+1 deoarece în Ne există un număr egal de electroni și un număr egal de protoni. Deci, din cauza sarcinii nucleare crescute, în comparație cu atomul neutru de Na, configurația stabilă a atomului de Na este perturbată și electronii sunt atrași spre nucleu.
La fel, de ce este Cl mai mare decât Na+? Na+ și Cl - Mărime relativă. In orice caz, Cl - înseamnă că există electroni în plus, care ar adăuga o forță de respingere între electroni și ar duce la o mai mare câmpul de electroni și a mai mare mărimea. Na+ îi lipsește un electron, astfel încât protonii au o strângere mai strânsă pe o cantitate mai mică de e-, rezultând o dimensiune mai mică.
De asemenea, trebuie să știți, de ce ionul Na+ este mai mic decât un atom neutru de Na?
Cel mai inteligent răspuns! ion Na+ este mai mic decât Na deoarece N / A își pierde singurul electron pentru a deveni ion Na+ astfel încât sarcina pozitivă a nucleului pe electron prezent va crește și rezultă că forța de atracție electrostatică crește. Prin urmare dimensiunea scade.
De ce este F mai mare decât Na+?
F numărul atomic este 9 având 9 electroni și 9 protoni. Deci în acele cazuri de Na+ , F -, Na+ este mai mică ca mărime datorită atracţiei electron-protoni dar F - este mai mare în mărime datorită repulsiei electron-electron în comparație cu atracția electron-proton..
Recomandat:
Care este cea mai mică particulă a unui element care păstrează proprietățile elementului?

Un atom este cea mai mică particulă dintre orice element care păstrează încă caracteristicile elementului respectiv. O bucată dintr-un element pe care o putem vedea sau manipula este formată din mulți, mulți atomi și toți atomii sunt la fel, toți au același număr de protoni
Care vine mai întâi lungimea sau lățimea sau înălțimea?
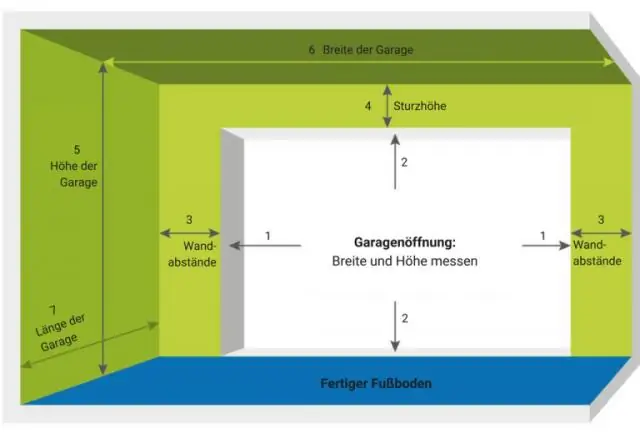
Ce vine mai întâi? Standardul industriei grafice este lățime cu înălțime (lățime x înălțime). Adică atunci când îți scrii măsurătorile, le scrii din punctul tău de vedere, începând cu lățimea. Asta este important
Care este orbital cu cea mai mică energie?

La cel mai scăzut nivel de energie, cel mai apropiat de centrul atomic, există un singur orbital 1s care poate conține 2 electroni. La următorul nivel de energie, există patru orbitali; un 2s, 2p1, 2p2 și un 2p3. Fiecare dintre acești orbitali poate deține 2 electroni, deci se pot găsi un total de 8 electroni la acest nivel de energie
Care este cea mai mică feriga?

Azolla caroliniana – o ferigă acvatică (dimensiune medie, 0,5–1,5 cm), este cea mai mică ferigă de pe pământ. Descoperirea noastră dezvăluie o nouă specie de ferigă cu limba viperă și o plasează printre cele mai mici ferigă terestre din lume, atingând o dimensiune medie de doar 1-1,2 cm
Care este cea mai mică lună a lui Jupiter?

Leda Pe lângă aceasta, Jupiter are 79 de luni? Planeta Jupiter acum are un total de 79 identificat luni . La mai bine de 400 de ani după ce Galileo Galilei a descoperit primul dintre lunile lui Jupiter , astronomi avea au găsit încă o duzină – inclusiv una pe care l-au numit „ciudat” – orbitând planeta.
