
- Autor Miles Stephen stephen@answers-science.com.
- Public 2023-12-15 23:40.
- Modificat ultima dată 2025-01-22 17:08.
Linii de emisie apar atunci când electronii unui atom excitat, element sau molecula se deplasează între nivelurile de energie, revenind la starea fundamentală. The linii spectrale a unui specific element sau moleculă în repaus într-un laborator apar întotdeauna la aceleași lungimi de undă.
În mod similar, se întreabă, ce înseamnă liniile de pe un spectru de emisie?
Linia de emisie . Un linia de emisie va apărea într-o spectru dacă sursa emite lungimi de undă specifice de radiaţie. Acest emisie apare atunci când un atom, un element sau o moleculă în stare excitată revine la o configurație de energie mai mică. Energia este egală cu diferența dintre nivelurile de energie superior și inferior.
Se mai poate întreba, de ce spectrul de emisie este format din linii discrete? Această eliberare are loc sub formă de lumină cu o anumită lungime de undă (culoare). Prin urmare, atomic spectre de emisie reprezintă electronii care se întorc la niveluri de energie inferioare. Fiecare pachet de energie corespunde unei linii din atom spectru . Nu există nimic între fiecare linie, așa că spectru este discontinuă.
De asemenea, care sunt lungimile de undă ale liniilor din spectrul de emisie de hidrogen?
Patru din Balmer linii sunt în partea „vizibilă” din punct de vedere tehnic a spectru , cu lungimi de undă mai lung de 400 nm și mai scurt de 700 nm. Părți din seria Balmer pot fi văzute în soare spectru . H-alfa este o linie importantă folosită în astronomie pentru a detecta prezența hidrogen.
Ce cauzează apariția liniilor într-un spectru de emisie?
The apariția liniilor într-un spectru de emisie este cauzat prin faptul că lumina este eliberată pe măsură ce un electron trece la o stare de energie mai scăzută. Când atomii absorb energie, se excită și ating un nivel mai înalt de energie.
Recomandat:
Cum sunt spectrele de emisie dovezi pentru învelișurile de electroni în modelul Bohr?

Prezența doar a anumitor linii în spectrele atomice a însemnat că un electron poate adopta doar anumite niveluri de energie discrete (energia este cuantificată); de unde ideea de învelișuri cuantice. Frecvențele fotonilor absorbite sau emise de un atom sunt fixate de diferențele dintre nivelurile de energie ale orbitelor
Ce cauzează spectrul de emisie al unui element?

Spectrele de emisie atomică apar din căderea electronilor de la niveluri de energie mai înalte la niveluri de energie mai scăzute în interiorul atomului, sunt eliberați fotoni (pachete de lumină) cu lungimi de undă specifice
Este spectrul de emisie atomică o gamă continuă de culori?

T/F Ca și spectrul vizibil, un spectru de emisie atomică este o gamă continuă de culori. T/F Fiecare element are un spectru unic de emisie atomică. T/F Faptul că doar anumite culori apar într-un spectru de emisie atomică a elementelor indică faptul că sunt emise doar anumite frecvențe de lumină
De ce este diferit spectrul de absorbție pentru clorofila a și spectrul de acțiune pentru fotosinteză?
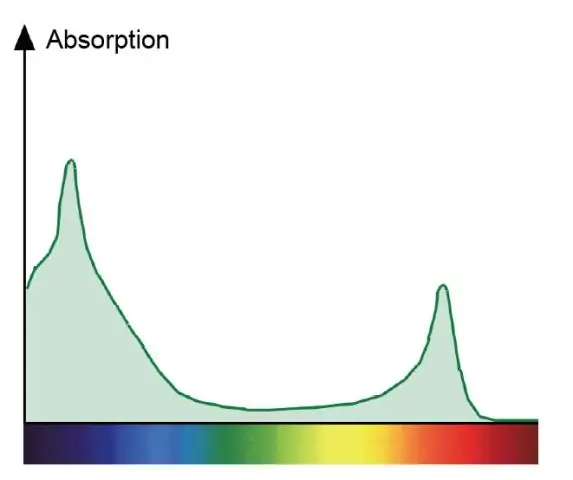
Un spectru de absorbție arată toate culorile luminii absorbite de o plantă. Un spectru de acțiune arată toate culorile luminii care sunt utilizate în fotosinteză. Clorofilele sunt pigmenții verzi care absorb roșul și albastrul și participă direct la fotosinteză
Care este spectrul de emisie al soarelui?

Spectrul de emisie al Soarelui. Soarele emite radiații electromagnetice pe o gamă largă de lungimi de undă. Maximul în spectrul de emisie solară este de aproximativ 500 nm, în partea albastru-verde a spectrului vizibil. Pe lângă lumina vizibilă, Soarele emite radiații ultraviolete și radiații infraroșii
