
Cuprins:
- Autor Miles Stephen stephen@answers-science.com.
- Public 2023-12-15 23:40.
- Modificat ultima dată 2025-06-01 05:05.
Cea mai comună formă a acestui lucru ecuaţie este deoarece PV= K și V/T =k atunci. PV/T = constant. Astfel, cel Ecuația gazelor ideale este dat ca. PV = nRT. unde P= presiunea gaz ; V=volumul gaz ; n= Numărul de alunițe; T = temperatura absolută; R= Gaz ideal constantă cunoscută și ca constantă Boltzmann = 0,082057 L atm K-1 mol-1.
În acest sens, cum deduceți ecuația gazului ideal?
Derivarea ecuației gazelor ideale
- Să considerăm că presiunea exercitată de gaz este „p”,
- Volumul gazului să fie - „v”
- Temperatura fie - T.
- n - să fie numărul de moli de gaz.
- Constanta universală de gaz - R.
- Conform legii lui Boyle,
De asemenea, știți, de ce se numește Legea gazelor ideale? Un gaz ideal este o gaz care se conformează, în comportamentul fizic, unei anumite relații idealizate între presiune, volum și temperatură numită legea gazelor ideale . A gaz nu se supune ecuației atunci când condițiile sunt astfel încât gaz , sau oricare dintre componente gazele într-un amestec, este aproape de punctul său de condensare.
Aici, ce se înțelege prin ecuația gazelor ideale?
ecuația gazelor . n. (Fizică generală) an ecuaţie care echivalează produsul dintre presiune și volumul unui mol de a gaz la produsul temperaturii sale termodinamice și a gaz constant. The ecuaţie este exact pentru un gaz ideal și este o bună aproximare în realitate gazele la presiuni joase.
Cine a creat legea gazelor ideale?
Robert Boyle
Recomandat:
Care este ecuația funcției pătratice?
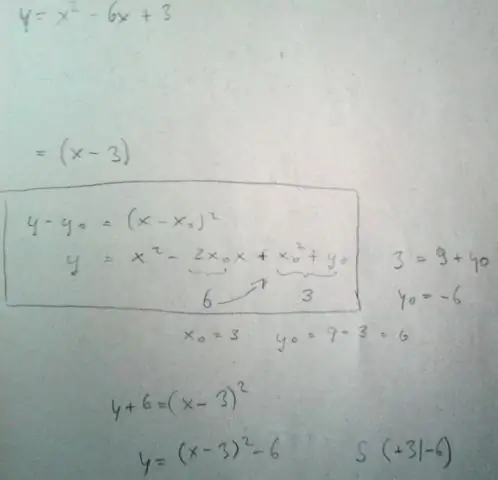
O funcție pătratică este una de forma f(x) = ax2 + bx + c, unde a, b și c sunt numere cu a diferit de zero. Graficul unei funcții pătratice este o curbă numită parabolă. Parabolele se pot deschide în sus sau în jos și variază în „lățime” sau „abruptă”, dar toate au aceeași formă de bază în „U”
Care este configurația gazului nobil al vanadiului?

Ar 3d3 4s2
Ce creează presiunea gazului și cum se modifică aceasta odată cu modificările energiei cinetice?

Presiunea gazului este cauzată de ciocnirile particulelor de gaz cu interiorul recipientului, când acestea se ciocnesc cu pereții containerului și exercită o forță asupra acestora. Apoi gazul este încălzit. Pe măsură ce temperatura gazului crește, particulele câștigă energie cinetică și viteza lor crește
De ce evadarea termică a gazului atmosferic este mult mai ușoară de pe Lună decât de pe Pământ?

De ce evadarea termică a gazului atmosferic este mult mai ușoară de pe Lună decât de pe Pământ? Pentru că gravitația Lunii este mult mai slabă decât cea a Pământului. Oxigenul eliberat de viață a fost îndepărtat din atmosferă prin reacții chimice cu rocile de suprafață până când roca de suprafață nu a mai putut absorbi
Care este ecuația unei drepte verticale care trece prin punctul (- 4 7?

Ecuația dreptei orizontale care trece prin (4,7) este y=7. Notă − Ecuația unei linii verticale este întotdeauna de tipul x=k și, prin urmare, ecuația dreptei verticale care trece prin (4,7) este x=4
