
- Autor Miles Stephen stephen@answers-science.com.
- Public 2023-12-15 23:40.
- Modificat ultima dată 2025-06-01 05:05.
Numărul lui Avogadro, numărul de particule din a cârtiță , poate fi determinat experimental prin „numărarea” mai întâi a numărului de atomi într-un spațiu mai mic și apoi mărirea pentru a găsi numărul de particule care ar avea o masă egală cu masa atomică sau moleculară în grame.
În mod similar, se poate întreba cum a fost dezvoltat conceptul de cârtiță?
Istoria cârtiță se împletește cu cea a masei moleculare, unităților de masă atomică, numărul Avogadro. Primul tabel cu greutatea atomică standard (masa atomică) a fost publicat de John Dalton (1766-1844) în 1805, pe baza unui sistem în care masa atomică relativă a hidrogenului a fost definită ca 1.
Se mai poate întreba, când a fost descoperită alunița? În general, unul cârtiță al oricărei substanțe conține Numărul lui Avogadro de molecule sau atomi ai acelei substanțe. Această relație a fost prima descoperit de Amadeo Avogadro (1776-1858) și a primit credit pentru aceasta după moartea sa.
Ținând cont de acest lucru, pe ce se bazează alunița?
Ca toate unitățile, a cârtiță trebuie sa fie bazat pe ceva reproductibil. A cârtiță este cantitatea de orice care are același număr de particule găsite în 12.000 de grame de carbon-12. Acest număr de particule este numărul lui Avogadro, care este de aproximativ 6,02x1023. 1? A cârtiță a atomilor de carbon este 6,02x1023 atomi de carbon.
De ce o aluniță este numită aluniță în chimie?
The cârtiță este o unitate folosită în chimie care este egal cu numărul lui Avogadro. Este numărul de atomi de carbon din 12 grame de izotop carbon-12. Cuvantul cârtiță provine de la cuvântul moleculă. The cârtiță este cel mai adesea folosit pentru a converti între numere de atomi și molecule în unitatea gram de masă.
Recomandat:
Cum găsiți derivata a doua a unei funcții trigonometrice?
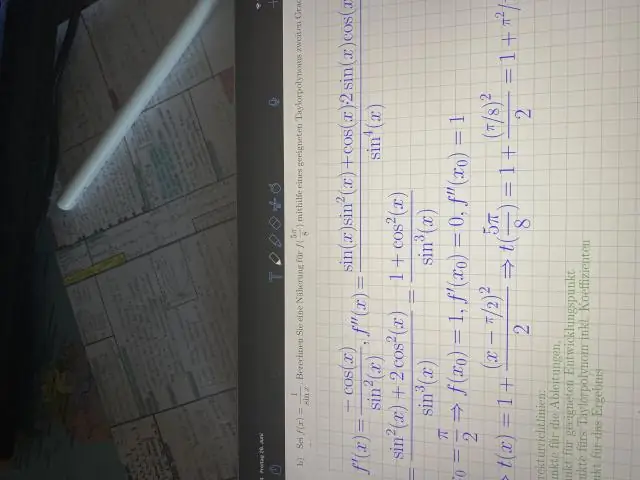
VIDEO Chiar așa, care sunt derivatele celor 6 funcții trigonometrice? Derivate ale funcţiilor trigonometrice. Funcțiile trigonometrice de bază includ următoarele 6 funcții: sinus ( păcat x), cosinus ( cos x), tangentă (tanx), cotangentă (cotx), secantă (secx) și cosecantă (cscx).
Câți ioni sunt într-o aluniță?

Alunița și numărul lui Avogadro. O mol dintr-o substanță este egală cu 6,022 × 10²³ unități ale acelei substanțe (cum ar fi atomi, molecule, orioni)
Care este abrevierea pentru aluniță?

Mole (abreviere, mol) este unitatea standard internațională (SI) a cantității de material. Un mol este numărul de atomi s în exact 12 miimi de kilogram (0,012 kg) de C-12, cel mai comun izotop natural al elementului carbon
Cum măsori o aluniță?

Dacă doriți să știți câți moli de material aveți, împărțiți masa materialului la masa sa molară. Numărul lui Avogadro este numărul de unități dintr-un mol dintr-o substanță sau 6,02214076 × 1023. Masa molară a unei substanțe este masa în grame a unui mol a acelei substanțe
Ce este o alunita matematica?

Mol. Mole este unitatea de măsură SI folosită pentru a măsura numărul de lucruri, de obicei atomi sau molecule. Un mol de ceva este egal cu 6,02214078×1023 din aceleași lucruri (numărul lui Avogadro)
